
oxaion easy Medizintechnik - Die Unternehmenssoftware...
Gerade kleinere Unternehmen in der Medizintechnik spüren den Druck, den die neue DIN EN ISO 134...
Digitale Medizintechnik-Messe des größten MedTech Clusters Deutschlands

oxaion easy Medizintechnik - Die Unternehmenssoftware...
Gerade kleinere Unternehmen in der Medizintechnik spüren den Druck, den die neue DIN EN ISO 134...
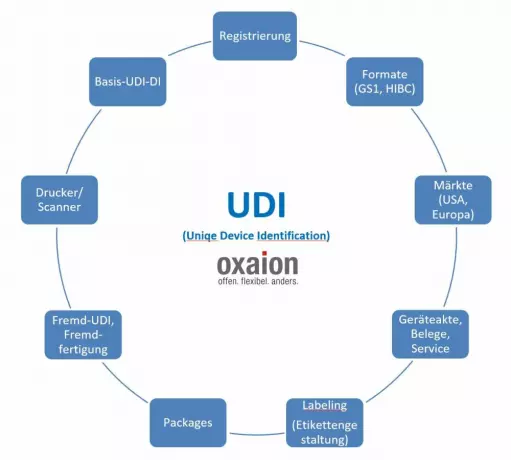
UDI als Teil der Unternehmenssoftware in...
Die UDI entwickelt sich nicht zuletzt durch die MDR zu einem wesentlichen Bestandteil übergreif...

UDI-Datenbanklösungen helfen Herstellern, die UDI-Vorschriften einzuhalten. Diese Kennungen sind eine Reihe von Zeichen, die unter Verwendung international anerkannter Standards erstellt wurden. UDI hilft Unternehmen bei der Identifizierung bestimmter Medizinprodukte auf dem Markt und erleichtert deren Überwachung durch die zuständigen Behörden. UDI ist für alle Medizinprodukte erforderlich, die den neuen europäischen Richtlinien MDR und IVDR unterliegen. Die GDSN-Datenbank wird von der Europäischen Kommission verwaltet und verfügt über eine zentrale Datenbank mit UDIs für alle Arten von Produkten.
UDI-Datenbanklösungen sind entscheidend für den Erfolg von Herstellern medizinischer Geräte. Das UDID-System wurde weltweit für alle Klassen von Medizinprodukten implementiert. Eine unabhängige Aufsichtsbehörde muss das System überwachen, um die Einhaltung und Einheitlichkeit sicherzustellen. Obwohl das UDI-System erstmals vor sechs Jahren in den USA eingeführt wurde, hat es sich noch nicht in allen Ländern weltweit durchgesetzt. Während sich das System weiterentwickelt, müssen die Hersteller die Änderungen der regulatorischen Anforderungen und der Technologie entsprechend planen.
UDI-Datenbanklösungen sind entscheidend für den Erfolg des UDI-Systems. Diese Lösungen können umfassende, zuverlässige und zeitnahe UDI-Daten liefern und Herstellern helfen, die UDI-Vorschriften einzuhalten. Beispielsweise ermöglicht die Lösung SingleSource (tm) von Reed Tech Unternehmen, UDI-Daten während des gesamten Produktlebenszyklus zu verwalten. Diese Lösung verfügt über mehrere UDI-Kanäle für die US-amerikanische FDA, die chinesische NMPA und die südkoreanische MFDS. Darüber hinaus unterstützt es die Bereitstellung für EU EUDAMED.
UDI ist in das Medizinprodukt, die IFUs und die Verpackung eingebettet. Es sollte für einzeln verpackte Geräte eindeutig sein und nicht für Geräte, die in Mehrfachverpackungen verkauft werden. Unterschiedlichen Verpackungsarten sollten für unterschiedliche Zwecke unterschiedliche UDIs zugeordnet werden. Ebenso muss die Anzahl der in einem Paket zusammengepackten Geräte unterschiedliche UDIs haben. Außerdem muss bei jeder Produktänderung eine neue UDI generiert werden.
UDI ist eine Anforderung für Medizinprodukte. Es wurde erstmals von der US-amerikanischen FDA eingeführt und von Aufsichtsbehörden auf der ganzen Welt übernommen. Ihr Hauptziel ist es, die Patientensicherheit zu verbessern und das Lieferkettenmanagement von Medizinprodukten zu verbessern. Seine UDI ist eine verschlüsselte, eindeutige Kennung, die zur Identifizierung des Produkts verwendet werden kann. Es sollte auf der Verpackung aufgedruckt sein. Wenn sich das Gerät auf einem physischen Datenträger befindet, sollte die UDI bei dem entsprechenden Artikel aufgezeichnet werden.
UDI-Datenbanklösungen sind ein wesentlicher Bestandteil eines regulierten Medizinprodukts. Sie können Unternehmen dabei helfen, die UDI-Vorschriften einzuhalten und sicherzustellen, dass ihre Produkte sicher sind. Eine UDI-Datenbanklösung ist ein wesentliches Element der Regulierung von Medizinprodukten. Mit UDI können Hersteller die Leistung ihrer Produkte verfolgen. Dadurch können sie ein besseres Geschäftsmodell entwickeln. Darüber hinaus hilft ihnen eine UDI-Datenbank, ihre Geräte zu verfolgen und zu überwachen und ihre Sicherheit zu verbessern.
Werden Sie selbst digitaler Aussteller im Online-Portal der größten und bekanntesten MedTech Cluster Region Deutschlands und informieren Sie die Welt der Medizintechnik über Ihre Produkte und Dienstleistungen sowie über News, Events und Karrieremöglichkeiten.
Mit einem ansprechenden Online-Profil, helfen wir Ihnen dabei sich professionell auf unserem Portal sowie in Google und in den sozialen Medien virtuell zu präsentieren.